動脈硬化症が重症化すると、心筋梗塞や脳卒中などが起こり、QOLや日常生活動作(ADL)が著しく損なわれ、命にかかわる問題が生じることがあります。
しかし、動脈硬化症をより早く発見して適切な治療を受けられる方法は確立していないのが現状です。動脈硬化症を単一の臓器や器官の病気ではなく、全身に影響をおよぼす病気として捉え、患者さん一人ひとりに発症前診断や重症化予測を行い、リスクが高い場合はより適切な治療を提供する先制医療を実現できることが理想です。
そこで、さまざまな医療研究機関や企業が参画した「動脈硬化性疾患を対象としたバイオマーカー開発を目指すプロジェクト」(以下、本プロジェクト)*が2020年に発足しました。本プロジェクトでは、血流に乗って全身の細胞に影響をおよぼす循環因子である細胞外小胞(extracellular vesicles:EVs)に着目しています。共同研究として、EVsに含まれる情報を解析した結果をもとに、動脈硬化症の発症あるいは重症化する前のリスクを予測できる方法や治療法の開発を目指しています。
旭川医科大学 外科学講座 血管・呼吸・腫瘍病態外科学分野(以下、旭川医科大学)が主導し、同大学が社会的価値や意義を有する研究事業に助成する「旭川医科大学社会的インパクト創出プロジェクト」にも採択された取り組みを中心に、研究の目的や意義、将来の医療への展望について分かりやすく紹介します。

旭川医科大学 外科学講座 血管・呼吸・腫瘍病態外科学分野 教授 旭川医科大学 副学長、旭川医科大学病院 病院長 日本血管外科学会 理事長 末梢動脈疾患ガイドライン作成合同研究班 班長
東 信良 先生
がん対策基本法に続き、2019年には循環器病対策基本法が制定されました。これは、循環器疾患がこれまで以上に国民の主要な死因として深刻化している現状を受けたものです。心臓や脳の血管に起こる動脈硬化はよく知られていますが、四肢末梢動脈の動脈硬化も深刻であり、歩行障害を来たして生活の質に悪影響をもたらすだけでなく、重度の動脈硬化症は、包括的高度慢性下肢虚血(いわゆる足の壊疽)といった重篤な疾患を引き起こします。末梢動脈の動脈硬化を有する場合、心筋梗塞や脳梗塞のリスクが高く、従って生命予後にも影響をもたらします。
これらの疾患は、複数の臓器にまたがって動脈硬化が進行する「重複動脈硬化症」として捉えることができ、全身的な視点からの理解と包括的な対策が求められています。従来、動脈硬化症は臓器ごとに個別の疾患として研究されてきましたが、近年では、それらが共通の循環因子を介して連動している可能性が注目されています。
私たちはこの点に着目し、血液中を循環する細胞外小胞の役割に関して、東京医科大学の落谷孝広先生と議論を重ねてまいりました。現在、旭川医科大学および東京医科大学を中心に、多施設共同研究データを基盤とした、細胞外小胞を用いた新たな動脈硬化症研究に取り組んでおります。
本研究は、旭川医科大学の社会的インパクト事業の一環として推進されており、地域から発信する先進的な医療研究が、世界の動脈硬化症対策に貢献することを目指しています。この取り組みが、重複動脈硬化症の理解と治療に新たな展望をもたらすことを願ってやみません。

東京医科大学 医学総合研究所
未来医療研究センター
分子細胞治療研究部門
特任教授
落谷 孝広 先生
循環器疾患は、がんに次いで本邦における死亡原因の第2位*1を占めており、医療費においても全医療費の約20%*2を占めるなど、医療資源が集中的に投入されている重要な疾患です。しかし、循環器疾患の発症には生活習慣病をはじめとするさまざまな要因が複雑に関与しており、個々の患者さんにおける発症を正確に予測することは、現在の医療では難しいとされています。
私たちはこれまで、がん分野においてノンコーディングRNAや細胞外小胞であるエクソソームの研究に取り組んできました。特に、エクソソームやその中に含まれるマイクロRNAに着目し、がんの発症、悪性化、転移に関わる分子メカニズムの解明を進めてきました。さらに、体液中を循環するエクソソームに含まれる分子を検出することで、リキッドバイオプシーによる診断法の研究・開発も行ってきました。
エクソソームはがん細胞だけでなく、さまざまな正常細胞からも分泌されることが知られています。そのため、がん研究で得られたエクソソームに関する知見は、循環器疾患においても疾患メカニズムの解明やバイオマーカーの開発に応用できる可能性があると考えています。
これまで私たちは、血液中に存在する微量な成分であるマイクロRNAの発現量を解析することで、がんを診断するシステムの研究・開発を進めてきました。本プロジェクトでは、これらの知見を基盤として、旭川医科大学、札幌ハートセンター、慶應義塾大学と連携し、血中細胞外小胞のマイクロRNAに着目した動脈硬化性疾患のバイオマーカー開発に取り組んでいます。
本プロジェクトでは、従来の画像診断や症状に基づく重症度分類とは異なり、病態をより直接的に反映する生物学的意義を持つバイオマーカーの開発を目指しています。これにより、将来的には発症予測や発症前診断を可能とする革新的な診断法の提供につなげたいと考えています。
旭川医科大学
外科学講座
血管・呼吸・腫瘍病態外科学分野
准教授
菊地 信介 先生

東京医科大学 医学総合研究所
未来医療研究センター
分子細胞治療研究部門
講師
吉岡 祐亮 先生

慶應義塾大学薬学部
創薬研究センター
ナノ医薬・分野横断遺伝学講座
教授
松崎 潤太郎 先生

医療法人札幌ハートセンター
理事
札幌心臓血管クリニック
院長/SHDセンター長
八戸 大輔 先生

旭川医科大学
外科学講座
血管・呼吸・腫瘍病態外科学分野
助教
栗山 直也 先生

旭川医科大学
外科学講座
血管・呼吸・腫瘍病態外科学分野
助教
鎌田 啓輔 先生

東京医科大学 医学総合研究所
未来医療研究センター
分子細胞治療研究部門
客員研究員
髙橋 一輝 先生

東京医科大学 医学総合研究所
未来医療研究センター
分子細胞治療研究部門
客員研究員
田丸 祐也 先生
動脈硬化症は、心臓から全身へ血液を届ける役割を持つ血管が硬くなったり、血管の内側が狭くなったりすることで臓器や器官に十分な血液が届かなくなることで発症します(図1)。
図1 動脈硬化症の発症メカニズム

動脈硬化症が重症化すると、QOLが著しく低下し、命にかかわる問題が生じることがあります。代表的な病気として、三大動脈硬化症が知られています(図2)。
心臓の動脈硬化症
冠動脈疾患(心筋梗塞など)
脳の動脈硬化症
脳血管疾患(脳梗塞などの原因による脳卒中)
足の動脈硬化症
下肢閉塞性動脈疾患
(Lower Extremity Artery Disease:LEAD)
三大動脈硬化症のなかで、心筋梗塞は胸の痛みや息苦しさが突然あらわれ、治療が成功しても心臓の筋肉にダメージが残り、心臓の機能低下を招くことがあります。脳卒中は、治療後も寝たきり状態となることが多いといわれています。足に起こる下肢閉塞性動脈疾患(動脈硬化性)のLEADは血流が悪くなることで歩くと足が痛くなる、傷が治りにくいといった症状が起こり、重症化すると足を切断することもあります。
これらの三大動脈硬化症は命にかかわることもある危険な病気です。心筋梗塞や脳卒中は日本人の死因のなかで上位の病気です。
図2 三大動脈硬化症
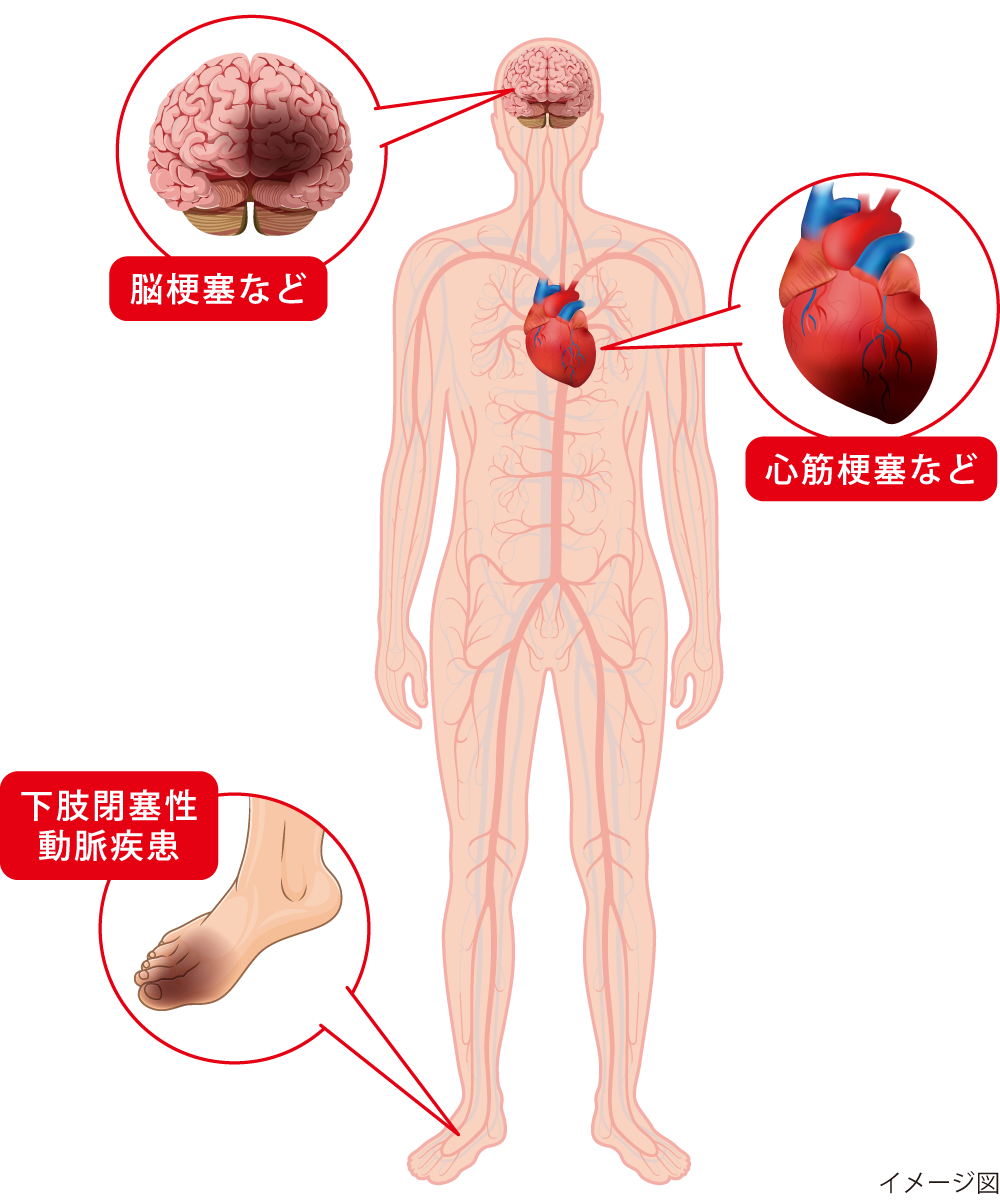
三大動脈硬化症は1つの臓器や器官だけではなく、心臓・脳・足など全身の臓器や器官に動脈硬化症が同時に起こることがあります。これは「重複動脈硬化症」と呼ばれています。
例えば、足に起こる下肢閉塞性動脈疾患(動脈硬化性)のLEADは国内の研究結果から冠動脈疾患や脳血管疾患の合併率が高いことが報告されています。医療者が診療の際に参考にしている「2022年改訂版 末梢動脈疾患ガイドライン」では、重複動脈硬化症が末梢動脈疾患を発症する「入り口」となる起因疾患として位置づけられています。
動脈硬化症の発症、ならびに三大動脈硬化症を予防することが必要です。予防対策は、バランスのよい食事、適度な運動、禁煙といった生活習慣の改善が重要といわれていましたが、生活習慣に気をつけていても、予防したり改善したりすることはハードルが高いのが現状です。
また、動脈硬化症は自覚がなく重症化するケースが多いのですが、診断の際に行われるCTやエコーを用いた画像検査では事前に予測することが難しいといわれています。また、がん治療のように原因に対して直接的に作用する薬剤は限られており、手術やカテーテル治療でも動脈硬化症を完全に防ぐことは困難であるといわれます。
発症・重症化を予測する検査方法の開発を目指しています
本プロジェクトでは、全身にわたって病気が進行し、画像検査では把握することが難しい動脈硬化症の発症・重症化リスクを事前に予測するために、バイオマーカーという目印を用いた検査方法に関する研究開発に取り組んでいます。
バイオマーカーとして、全身をめぐる血管を通じて各臓器に影響をおよぼす可能性がある細胞外小胞(EVs)という循環因子に注目しています(図3)。
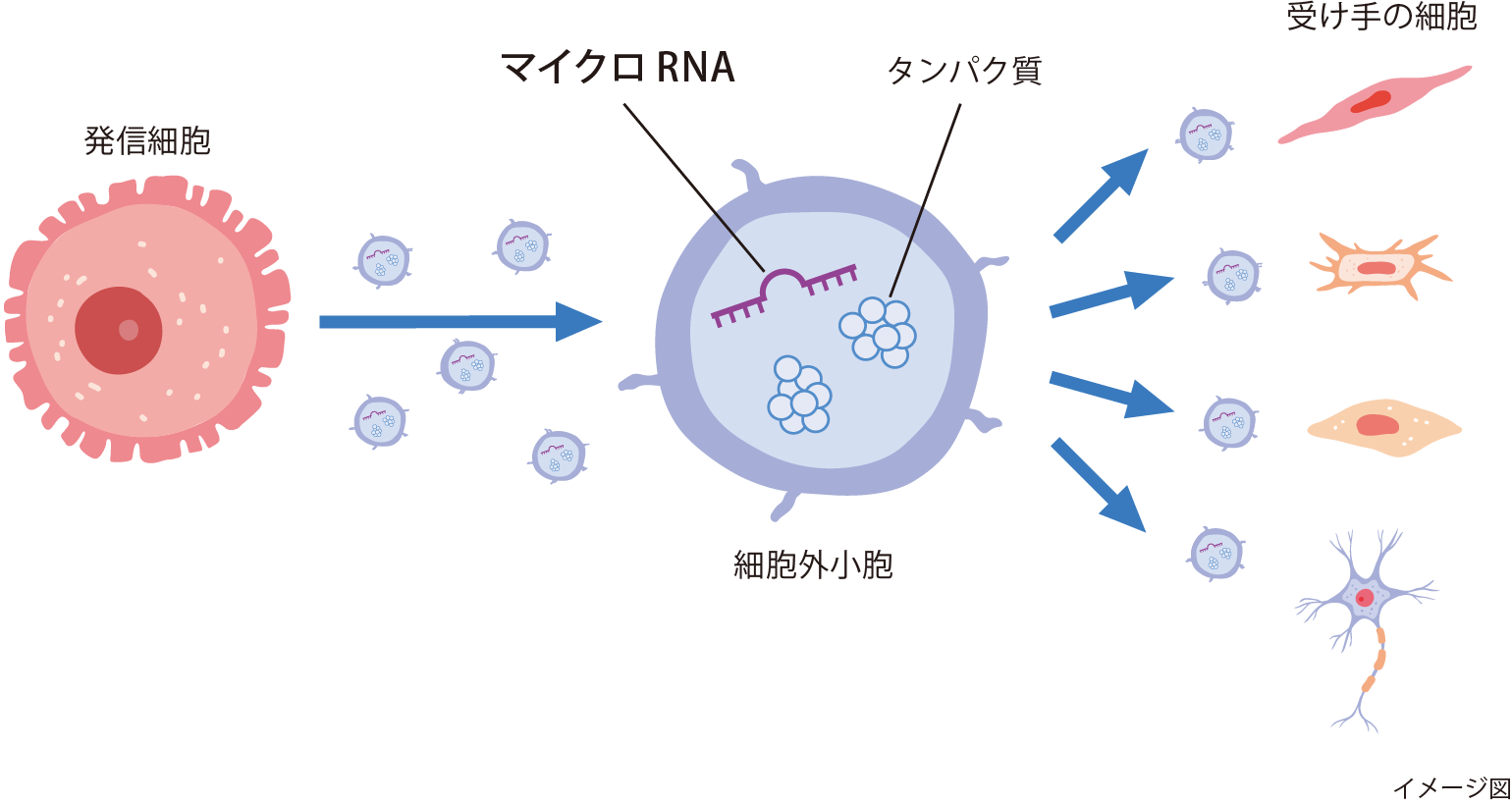
EVsは血液や体液のなかに存在する非常に小さいカプセル状の粒子で、EVsに含まれているマイクロRNAという分子やタンパク質が、各臓器・器官の細胞の働きに影響をおよぼす生物学的メッセンジャーの役割があることが、これまでの研究成果から示されています。
本プロジェクトでは、動脈硬化症が起こった臓器や器官の細胞から放出されたEVsが血流に乗って全身を循環したときに、EVs内のマイクロRNAが動脈硬化症の重複性に関わると考えています(図4)。
図3 全身をめぐる血管を通じて影響をおよぼす細胞外小胞
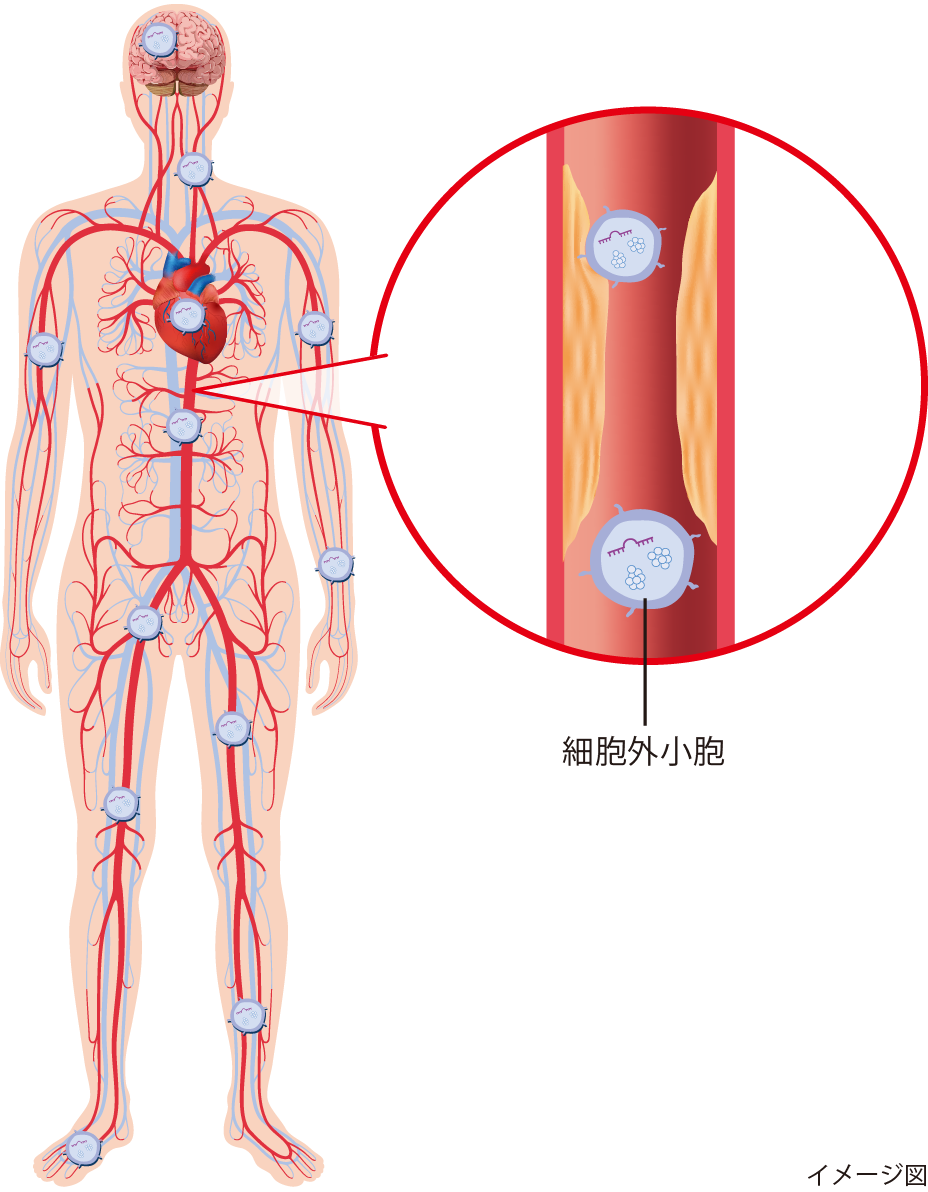
図4 動脈硬化症の重複性に関与する細胞外小胞とマイクロRNA
細胞外小胞(EVs)は、がん領域をはじめ、さまざまな病気に対する診断に有用と考えられています。本プロジェクトの共同研究機関である東京医科大学医学総合研究所 未来医療研究センター 分子細胞治療研究部門は、EVs内に含まれるマイクロRNAをがん診断に応用し、血液や体液を用いて遺伝子の異常などを解析するリキッドバイオプシーという低侵襲な検査方法の研究開発に取り組んでいます。
本プロジェクトでは、同大学において実証されつつあるEVsの診断的有用性の研究知見をもとに、血液検査だけで動脈硬化症の発症・重症化リスクを正確に見極められるリキッドバイオプシー検査の実用化を目指しています。
この検査方法が確立できれば、そもそも動脈硬化症を発症しやすい人なのかどうか、どの臓器に動脈硬化症が重複して重症化しやすいのかなどを予測することが可能と考えています。そして、発症前あるいは重症化する前に、一人ひとりに見合う適切な先制医療を提供し、医療費を最小限に抑えられることを実現したいと考えています。
旭川医科大学の革新的取り組み
旭川医科大学社会的インパクト創出プロジェクトにも採択
旭川医科大学は、三大動脈硬化症に対して細胞外小胞(EVs)をバイオマーカーに応用するための研究を実施してきました。
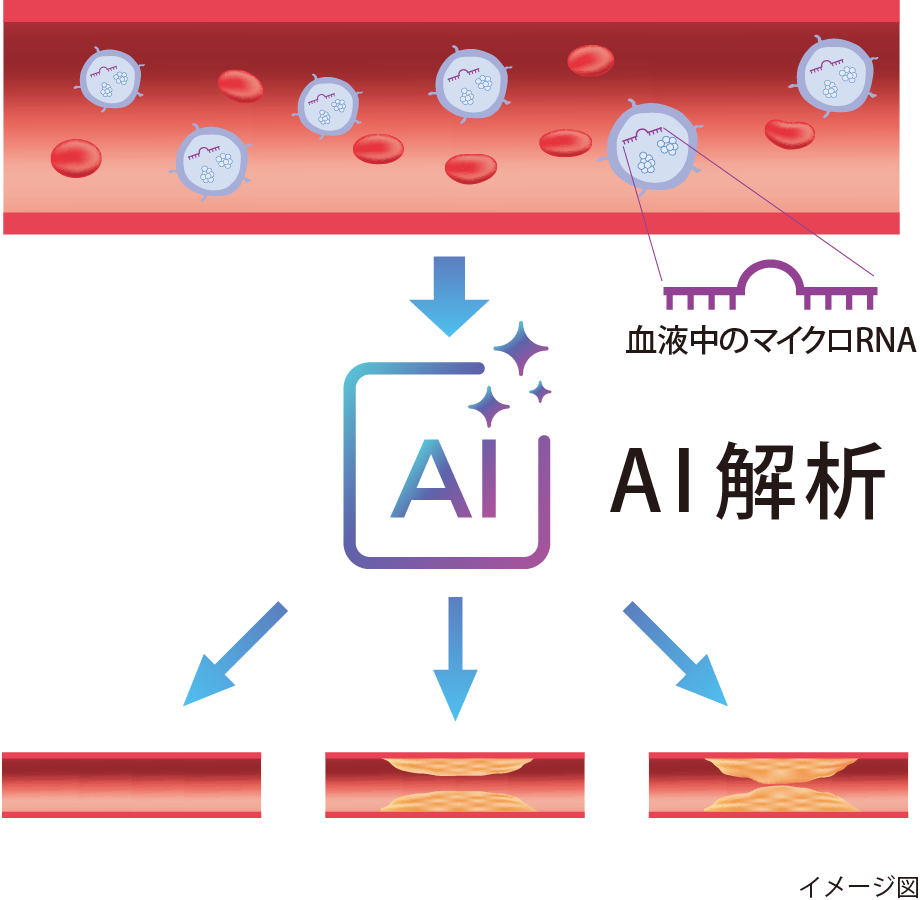
これらの研究のなかで、SOMPOホールディングスからの委託研究は、EVs内のマイクロRNAの発現パターンと病態との関係性をAI(機械学習)で明らかにして診断モデルを構築するために、多施設共同研究として展開しています。現在、約800例の症例解析を実施しており、日常臨床への実装を目指す段階にあります(図5)。また、この研究は同大学が社会的価値や意義を有する研究事業に助成する「旭川医科大学社会的インパクト創出プロジェクト」に採択された事業の1つです*。
三大動脈硬化症に対して細胞外小胞内マイクロRNAの発現パターンと病態との関係性をAI(機械学習)で結びつける診断モデル
旭川医科大学社会的インパクト創出プロジェクトで採択された研究事業
動脈瘤破裂を防ぐための早期診断・治療法の確立も目指しています
細胞外小胞(EVs)を応用する研究は、三大動脈硬化症以外にも拡げています。例えば、腹部大動脈瘤の新たな早期診断法や治療法の開発も視野に入れています*。
腹部大動脈瘤は、大動脈が正常の大きさから1.5倍以上の瘤状に膨らんだ状態で、50歳以上の男性に起こりやすいといわれています。自覚症状があらわれにくいので、スクリーニング検査や人間ドックで検査を受けないと発見されにくいといわれています。
一方で、動脈瘤が破裂した場合の死亡率が非常に高いことが問題です。より早く病気を発見して適切な治療につなげることが何よりも大切です。また、国内外で治療薬の研究開発が行われていますが、まだ実用化には至っていません。
こうしたなか、最近では動物実験の結果からEVsが動脈瘤の進行を抑えることにかかわる可能性が示されています。今後、患者さんの検体を用いてEVsやEVsに含まれるマイクロRNAを解析して病態を明らかにし、簡便な血液検査の方法や新しい治療法を開発することを目指しています(図6)。
腹部大動脈瘤の病態や移植後の血管が狭くなる現象を遺伝子レベルで解明する研究も推進しています
旭川医科大学は米国ワシントン大学血管外科学(以下、ワシントン大学)と連携し、腹部大動脈瘤や足に起こる下肢閉塞性動脈疾患(動脈硬化性、LEAD)の病態を明らかにするための研究に取り組んでいます。以下、細胞外小胞(EVs)を応用していない連携研究で明らかにされた知見を紹介します*。
腹部大動脈瘤に関しては家族歴が発症に関係しており、動脈硬化症を抑える方向に働く遺伝子と考えられるCDKN1B(以下、p27遺伝子)の発現が少ない人では、血管の狭窄が起こりやすいという研究報告があります。そこで、ワシントン大学との連携研究でp27遺伝子に着目したマウス実験を行いました。結果、p27遺伝子の発現量が少ないと、腹部大動脈瘤が形成されて病態が進行しやすく、破裂リスクが高い可能性があるという研究知見が得られました。
LEADに関しては、病変部を迂回する道をつくる手術において患者さん本人の血管を移植した後に、移植した血管が狭くなる現象が起こることについて、現象を解明するために血管が構成される内膜、中膜、外膜の3つの層の働きがそれぞれ異なることに着目して連携研究を行っています。
具体的には、旭川医科大学病院で手術を行い、その後に血管が狭くなる現象が起こった患者さんから、狭くなった血管と正常な血管が連続している組織を採取し、解析を行うワシントン大学に送ります。ワシントン大学では、血管の3つの層それぞれにおける遺伝子発現を把握することを可能とする空間的トランスクリプトーム解析を行ってもらいます(図7)。2026年2月時点の研究成果として、狭くなった血管と正常の血管との間で遺伝子発現が異なることがわかり、血管が狭くなる現象にかかわる複数の遺伝子を同定しました。
今後は最先端技術をもつ海外研究施設と連携できる強みを活かし、EVsを応用した研究を展開していく予定です。







